大塚製薬株式会社
4歳以上の部分発作を有するてんかん患者さんの服薬継続に寄与 「イーケプラ®点滴静注500mg」12月1日に国内販売開始
- 「イーケプラ®点滴静注 500mg」は、経口投与が一時的に困難な患者さんに対して「イーケプラ®」の継続した治療を可能とするために開発した。てんかん患者の部分発作の治療薬として、錠剤、ドライシロップに加え3剤形目となる
- てんかんは約100人に1人が発症し、小児期と高齢期の発症率が特に高い。抗てんかん薬の服薬を継続できれば約7割の患者さんは発作のない生活を送ることが可能となる。よって、経口摂取ができない患者さんには代替投与経路として注射剤が必要であり、この度新たな治療の選択肢となる
- 「イーケプラ®」の経口剤は、日本では2010年に発売され、既に10万人以上に使用されているが、注射剤は欧米で2006年に承認を取得しており、40以上の国又は地域で承認されている
大塚製薬株式会社(本社:東京都、代表取締役社長:樋口達夫、以下「大塚製薬」)とユーシービージャパン株式会社(本社:東京都、代表取締役社長:神原政信、以下「ユーシービージャパン」) は、「イーケプラ®点滴静注500mg」(一般名:レベチラセタム」)を12月1日に国内販売しますのでお知らせいたします。
「イーケプラ®点滴静注」の効能・効果は、経口投与ができない場合の一時的な代替製剤として経口製剤「てんかん患者の部分発作(二次性全般化発作を含む)」に準ずるものです。
てんかんは、乳幼児から高齢者まで幅広い年代で発症する病気で、国や地域によって性別や人種による発症率に大きな違いはなく、およそ100人に1人という発症頻度です。日本には約100万人のてんかん患者さんがいると言われていますが、適切な診断と薬物治療によりおよそ70%の患者さんはてんかん発作のない通常の生活を送ることができます。また、高齢で発症するてんかんの原因は脳卒中が30~40%と最も多く、次いでアルツハイマー病などの神経変性疾患や頭部の外傷、脳腫瘍などが挙げられます。
こうしたてんかんの薬物治療は長期にわたることから、胃腸障害や手術などで一時的に経口投与ができない場合でもてんかんに対する継続的な「イーケプラ®」の治療が必要であり、代替投与経路として注射剤を開発し、このたび本邦に於いても患者さんに提供できるようになりました。現在、レベチラセタム(海外での製品名Keppra®)の注射剤は、欧州、米国では2006年に承認を取得し、40以上の国・地域で承認されています。
大塚製薬とユーシービージャパンは、「イーケプラ®」を共同開発・販売していく中で、患者さんをサポートできるよう剤形を追加・改良してきました。更に強直間代発作の効能効果の追加を目指し承認申請中です。今後もてんかん治療をはじめとする中枢神経疾患の治療に貢献してまいります。
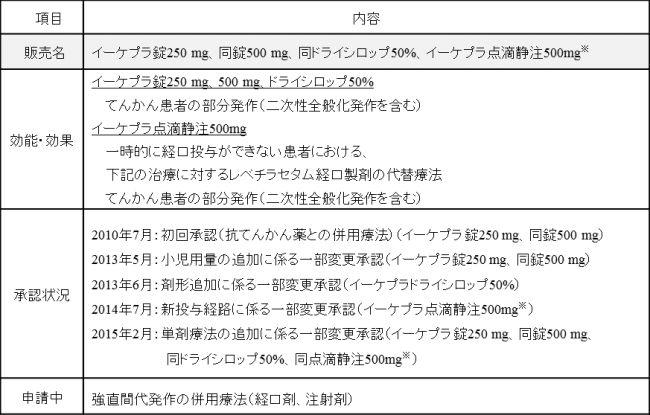
参考資料:日本におけるイーケプラの開発・申請・承認状況
イーケプラ®について
「イーケプラ®」は、1980年代初期にユーシービー社(ベルギー)で発見された中枢作用物質で、従来の抗てんかん薬と異なる作用機序を有する抗てんかん薬です。海外ではKeppra®のブランド名で発売され、全世界で600万人の使用経験がある抗てんかん薬で1999年に米国、続いて2000年に欧州で発売されています。経口剤については2013年1月現在、「成人てんかん患者の部分発作に対する併用療法」の適応では、欧米をはじめ100以上の国・地域で承認され、「小児てんかん患者の部分発作に対する併用療法」の適応でも80以上の国または地域で承認されており小児に対しても広く使用されています。注射剤は、欧米で2006年に承認を取得、40以上の国又は地域で承認されています。
日本では「イーケプラ®」として2010年9月から成人てんかん患者の部分発作に対する併用療法で発売され、小児てんかん患者の部分発作に対する併用療法として錠剤の適応が2013年5月に、ドライシロップが同年6月に、更に点滴静注が2014年7月に追加承認されました。また2015年2月に単剤療法の承認を取得し、部分発作を有する4歳以上の患者さんへの使用が可能となりました。
なお欧米では、成人部分発作だけでなく、強直間代発作及びミオクロニー発作に対する併用療法や乳幼児の部分発作に対する併用療法についても追加承認されました。また欧州では、成人てんかん患者の部分発作に対する単剤療法としても承認されています。
てんかんについての情報
てんかんinfoをご覧ください。2014年4月よりリニューアルし、てんかん発作の動画(イメージ)をみることができます。
また、てんかん治療における医師とのコミュニケーションに役立つてんかん発作日誌アプリのEpi Diaryもご参照ください。






