大塚製薬株式会社
抗精神病薬「エビリファイ®錠1mg」国内で新発売
- 当社創製の抗精神病薬「エビリファイ」の追加規格「エビリファイ®錠1mg」を11月29日に国内発売
- 「エビリファイ」の4つ目の適応となる「小児期の自閉スペクトラム症に伴う易刺激性」の追加効能の承認を9月に取得。1mg錠は本追加効能の投与開始用量となる
- 「エビリファイ」は、米国で2009年に小児患者さんに対する「自閉性障害に伴う易刺激性」の承認を取得。日本でも必要性の高い薬として小児関連学会からの開発要望を受け、厚生労働省から開発要請があった
大塚製薬株式会社(本社:東京都、代表取締役社長:樋口達夫、以下「大塚製薬」)は、抗精神病薬「エビリファイ(一般名:アリピプラゾール)」の追加規格として「エビリファイ®錠1mg」を11月29日に日本で発売します。「エビリファイ」は、本年9月に「小児期の自閉スペクトラム症に伴う易刺激性」の適応症を取得しました。1mg錠はその投与開始用量となります。
自閉スペクトラム症は、国内には約10万人の患者さんがいるといわれています※1。コミュニケーション障害、対人関係・社会性の障害、パターン化した行動などの症状があります。そのうち一部の患者さんでは、かんしゃく、攻撃性、自傷行為、またはこれらの複合行為の行動障害(易刺激性)を呈することがあるといわれており、患者さん自身や家族に重大な影響を及ぼす場合があります。しかしそれらの易刺激性に対して安全に使用できる薬は少なく、また特に小児期では、薬の服用に伴う体重増加や眠気など学業への影響も配慮する必要がありました。
「エビリファイ」は、米国で2009年に小児患者さんに対する「自閉性障害に伴う易刺激性:Irritability associated with autistic disorder」の適応症を取得しました。日本では、2011年に日本小児心身医学会、日本小児精神神経学会、日本小児神経学会の3学会より医療上の必要性の高い未承認薬・適応外薬検討会議に開発要望が出され、2012年に当社は厚生労働省より開発要請の通知を受けました。
こうした背景から、日本でも易刺激性を伴う自閉性障害の患者さん(6~17歳)を対象に臨床試験を実施し、2016年9月に承認を取得しました※2。
大塚製薬は、今後も世界中の未解決の医療ニーズを満たすため、精神疾患、神経疾患、がんを最重点領域とした研究開発を進めてまいります。
- 1平成26年患者調査(厚生労働省) 総患者数、傷病基本分類別のうち、「自閉症」、「非定型自閉症」、「アスペルガー〈Asperger〉症候群」、「その他の広汎性発達障害」「広汎性発達障害,詳細不明」の患者数を足し合わせた数値
- 22013年に米国精神医学会「精神疾患の診断・統計マニュアル(DSM)」の改訂により診断名が変更されたため、承認を受けた適応症は「自閉スペクトラム症」となっています。
製品写真
参考資料
自閉スペクトラム症について
自閉スペクトラム症は、発達障害の1つとして位置づけられています。2013年に米国精神医学会「精神疾患の診断・統計マニュアル(DSM)」が更新され、それまで広汎性発達障害に含まれていた自閉性障害、アスペルガー障害などが自閉スペクトラム症と称されるようになりました。
自閉スペクトラム症の原因は脳の機能障害に関係があるといわれていますが、特定はされていません。治療は、薬物療法の前に行動療法などが優先されて行われます。病気に伴う行動障害については、いくつかの神経伝達物質が関与し、中度から重度の行動障害にはドパミン神経系の関与があることがわかっています※3。抗ドパミン作用を持つ抗精神病薬は、興奮性(易刺激性)に対し有効であることが確認されており※4、一般的に抗ドパミン作用を主体とした抗精神病薬が経験的に頻用されています。米国では自閉性障害に伴う易刺激性に対して2006年に初めて非定型抗精神病薬※5が承認され、2009年には「エビリファイ」が同適応症の承認を取得しています。日本では1982年に定型抗精神病薬※5が自閉性障害の異常行動などに対して承認されましたが、副作用が多いことから小児の患者さんが使用するうえで安全性の課題がありました。その後、非定型抗精神病薬も国内承認を受け、薬物療法の選択肢が増えています。
すまいるナビゲーター「子どもの自閉スペクトラム症」もご参照ください。
- 3森 健治; 自閉症スペクトラムへの対応-児の将来を念頭に 医療的対応.脳と発達, 42, 199-203, 2010
- 4鈴木 勝昭, 杉山登志郎;自閉症スペクトラムと脳, BRAIN MEDICAL, 24(4), 309-16, 2012
- 5抗精神病薬は、定型抗精神病薬(従来型)と非定型抗精神病薬(新規)とに分けられます。非定型抗精神病薬は、副作用の錐体外路症状(手がふるえる、体が硬くなるなど)が少ないなどの特徴があります。(すまいるナビゲーター参照)
「エビリファイ」について
「エビリファイ」は、大塚製薬が1988年に発見、開発し、2002年に統合失調症治療薬として米国で承認を取得後、現在日本を含めた60以上の国と地域で使用されています。ドパミンパーシャルアゴニスト作用という新しい薬理作用を持ち、脳内でドパミンが過剰に放出されているときには抑制的に働き、ドパミンが少量しか放出されていないときには刺激する方向で作用し、結果としてドパミン神経を安定化させます。
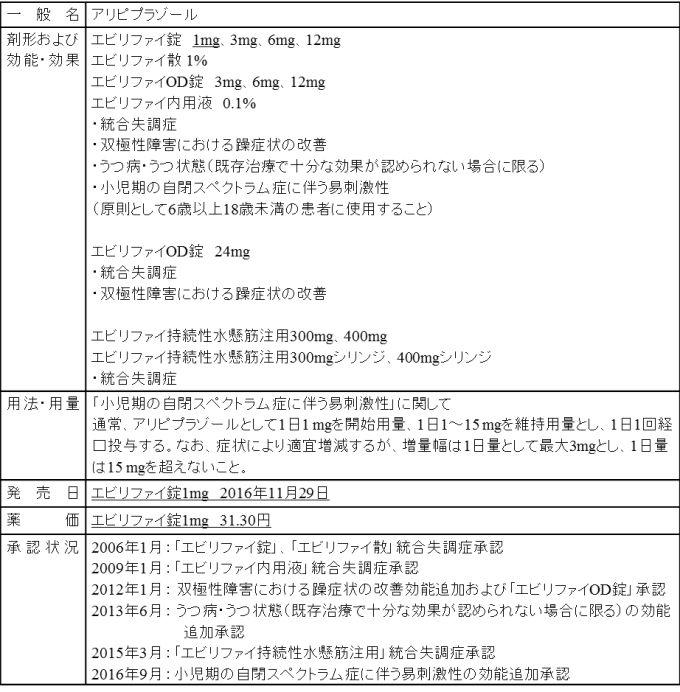
国内における承認状況(下線が今回の追加部分)