創薬プラットフォームの強化
医薬品の研究は、病気の原因と考えられる分子(タンパク質)を特定することから始まり、特定された分子に結合して異常な働きを抑える化合物が医薬品の候補となります。しかし、その候補化合物を見つけて絞り込むには多くの実験が必要です。大塚製薬では新たな創薬技術を積極的に取り入れることで、より幅広いターゲットに対して効率的に医薬品の候補化合物を創出できる環境を整備しています。
クライオ電子顕微鏡


ターゲットとなる分子(タンパク質)の構造を解明するために、従来はX線結晶構造解析という方法が主に用いられてきました。しかし、このX線結晶構造解析では、構造を決定するのにタンパク質を結晶化する必要があり、そのプロセスに長い年月かかることもあるなどの課題も存在します。
クライオ電子顕微鏡による構造解析技術は、タンパク質の結晶化が不要で汎用的に使うことができる技術として普及してきています。特に今まで結晶化が困難だったターゲット分子の構造解析がクライオ電子顕微鏡で可能となり、創薬研究期間の短縮とともに、より幅広い疾患へのアプローチができるようになりました。
大塚製薬でもクライオ電子顕微鏡の技術に早くから着目してきました。
大塚製薬の英国子会社アステックス社が2016年に欧州クライオ電子顕微鏡コンソーシアムに中心企業の1つとして参画し、クライオ電子顕微鏡を利用した創薬を本格的に開始しました。2017年にはアステックス社がクライオ電子顕微鏡を導入し、現在では豊富な経験と実績を有しています。
国内でも2022年の大阪創薬研究センターの設立に伴い、クライオ電子顕微鏡を導入し、アステックス社と技術的な部分で連携しながら、研究基盤の強化を進めています。
アステックス社は、ヨーロッパでは初の試みである“製薬企業によるクライオ電子顕微鏡コンソーシアム”の設立に主導的な役割を果たしてきました。アステックス社は、コンソーシアム参画製薬企業5社とともにクライオ電子顕微鏡をMRC-LMB(英国MRC分子生物学研究所)、ケンブリッジ大学の研究者とともに初期創薬研究に使用しています。
デジタルクライオ創薬
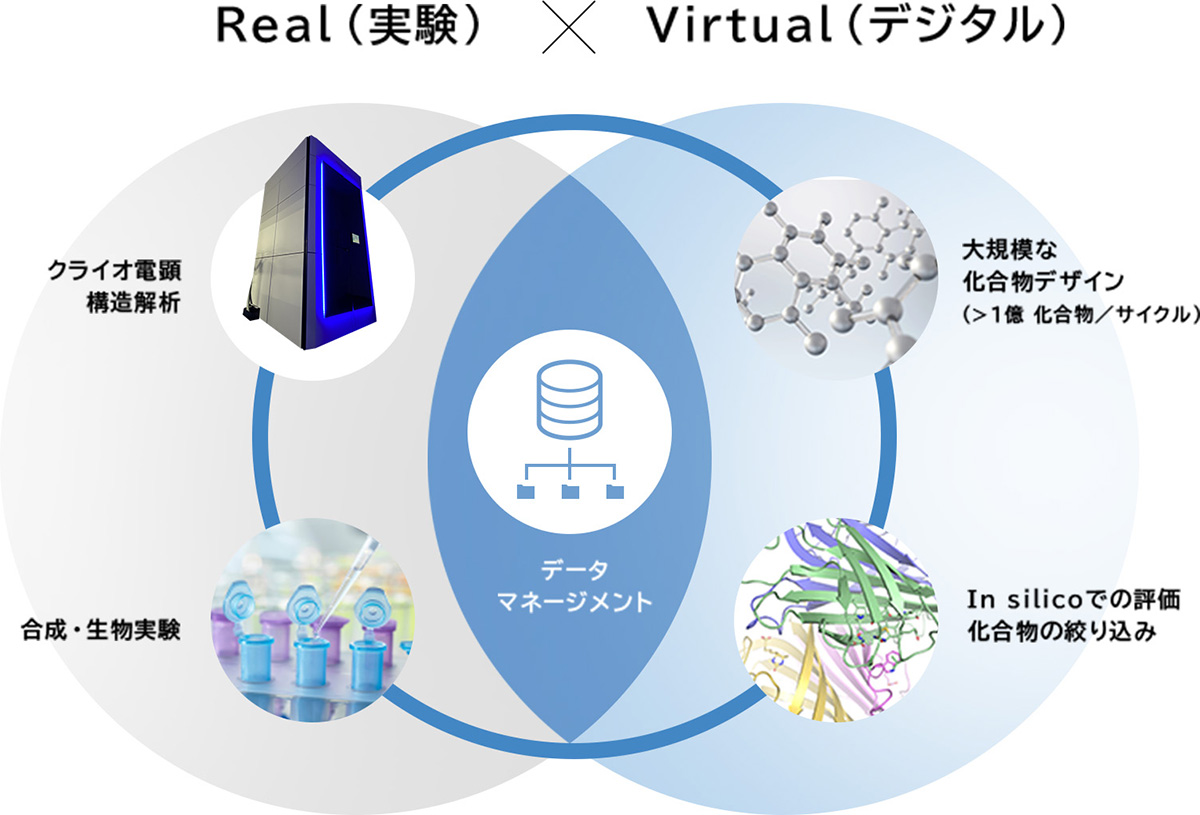
大塚製薬ではクライオ電子顕微鏡等から得られた構造情報を基に、AIやデジタル技術を活用して大規模な化合物デザインの作成と薬剤としての活性や物性の評価を行い、有望な化合物の絞り込みを行っています。
物理学に基づく計算プラットフォームの先駆者であり、大塚製薬とアステックス社が創薬共同研究を行っているシュレーディンガー社は、より迅速かつ低コストで、医薬品開発および材料用途の高品質な新規分子の発見を可能にしています。
多様性かつスピード感を有する化合物プロセスを何度も繰り返すことで、短期間に新規性を有する高活性な薬剤候補化合物の創出を目指します。